成都奥创生物参与了名为《CaO2 nanoparticle-loaded injectable hydrogel with sustained oxygen release and ROSscavenging functions for accelerating frostbite wound healing at high altitude》的实验项目,这项研究为高海拔地区的冻伤修复提供了一种有前景的策略,具有巨大的潜在临床应用价值。
1、文章:
CaO2 nanoparticle-loaded injectable hydrogel with sustained oxygen release and ROSscavenging functions for accelerating frostbite wound healing at high altitude
一种用于促进高海拔地区冻伤伤口愈合的具有持续释氧和清除活性氧功能的过氧化钙纳米粒子负载型可注射水凝胶研究
NANOSCALE
DOI: 10.1039/d5nr05331e
2、挂名引用:
3、期刊介绍:
期刊名:BIOSENSORS & BIOELECTRONICS
2025年影响因子/JCR分区:5.1/Q1
学科与分区:
材料科学(Q3);
CHEMISTRY, MULTIDISCIPLINARY(Q3);
MATERIALS SCIENCE, MULTIDISCIPLINARY(Q3);
NANOSCIENCE & NANOTECHNOLOGY(Q3);
PHYSICS, APPLIED(Q3)。
出版国家或地区:ENGLAND
冻伤在高海拔地区十分普遍,且与低海拔地区相比,恶劣的环境条件使冻伤创面更易发展为慢性难愈性伤口。 冻伤导致的血管损伤会阻碍氧气输送,造成伤口局部缺氧环境,而高海拔地区的低氧水平进一步减少供氧量,加剧组织缺氧并限制愈合。此外,持续缺氧叠加高海拔地区的寒冷气候与强烈紫外线辐射,会显著提高伤口中活性氧水平,导致严重氧化应激和组织损伤。 因此,高海拔冻伤创面极易陷入缺氧与过量活性氧的恶性循环,大幅增加发展为难愈性伤口的风险。为促进缺氧伤口愈合,临床上广泛采用吸氧和高压氧治疗等全身氧疗方式,但这些疗法存在氧中毒风险,且停止治疗后伤口氧含量会迅速下降,总体疗效并不理想。
为解决这些问题,局部释氧敷料通过整合产氧成分(如藻类、过氧化物)或载氧体(如血红蛋白、全氟化碳)实现了直接向创面输送氧气。在此类敷料所用材料中,纳米级过氧化钙(CaO2)颗粒因其低成本及能与水发生无催化反应产氧的特性而备受关注。但是,这种产氧机制会导致仅持续3-5天的爆发式氧释放,而该持续时间不足以满足伤口修复过程中血管生成、上皮再生和细胞外基质合成所需的持续供氧(此过程通常需约2周或更长时间)。此外,由此产生的短暂高氧状态会进一步加剧伤口组织中活性氧的过度积累。因此,设计能调控CaO2分解同时具备清除活性氧能力的合适载体,将有利于高海拔冻伤治疗敷料的临床开发。
可注射自修复水凝胶已成为构建多功能伤口敷料的通用载体。这类水凝胶的关键优势包括:具有类似细胞外基质(ECM)的结构、能够负载多种生物活性剂、以及可注射性使其能精准填充不规则创面。研究人员开发出将产氧过氧化物与活性氧(ROS)清除酶整合的可注射水凝胶敷料,用于治疗糖尿病创面、感染创面和烧伤创面等缺氧性伤口。在这些系统中,三维水凝胶网络可限制产氧过氧化物的分解,从而维持持续氧释放,同时负载的酶能清除过量活性氧。这两种效应共同作用显著促进了缺氧伤口的愈合。尽管可注射水凝胶具有多种优势及广泛的应用场景,但在高海拔缺氧性冻伤创面的应用仍面临挑战。具体而言,传统水凝胶缺乏抗冻性与低温粘附性,因此容易冻结、变脆并从伤口表面脱落,限制了其使用和储存。此外,冰晶形成会降低活性氧清除酶的活性并阻碍氧气输送,进一步制约治疗效果。虽然盐溶液和离子液体被广泛用作抗冻剂,但其较差的生物相容性、高流动性和不稳定性限制了它们在生物医学领域的应用。因此,理想的高海拔冻伤用可注射水凝胶敷料应兼具生物相容性、优异抗冻性能和强低温粘附力,以确保功能可靠性。
为满足高海拔冻伤创面的治疗需求,实验室开发了一种由聚乙烯吡咯烷酮(PVP)稳定的CaO2纳米颗粒(CPO NPs)与聚乙烯醇(PVA)构成的多功能水凝胶(CPO-PTG),并添加了两种生物相容性组分:单宁酸(TA)和甘油(Scheme 1A)。 TA是一种天然生物相容性多酚化合物,具有强效抗菌、活性氧清除和抗炎特性。TA丰富的羟基基团通过多重共价和非共价相互作用,能够稳定粘附于多种材料表面。甘油可作为抗冻剂使用,因其能与水形成致密的氢键网络,从而降低冰点并抑制冰晶形成。因此,甘油已作为冷冻保护剂广泛应用于食品、化妆品及细胞/器官低温保存系统。新型水凝胶的四种组分构成多重动态氢键网络,赋予材料剪切稀化和自修复特性,既能通过注射方式递送至不规则创面,又可保持结构完整性。得益于甘油介导的低温保护作用增强了TA与组织表面间的多价相互作用,CPO-PTG水凝胶在零下温度仍保持柔韧性并展现强效粘附性能。 同时,TA赋予水凝胶抗菌活性,这对预防伤口感染至关重要。此外,该水凝胶网络可调控CPO NPs的氧气释放速率,并与TA的ROS清除活性协同作用,在体外缺氧条件下促进细胞增殖和管腔形成。 CPO-PTG水凝胶促进伤口愈合的体内功效已通过大鼠冻伤诱导的缺氧伤口模型得到验证(示意图1B)。可以预见,CPO-PTG水凝胶将成为治疗高海拔冻伤创面的一种极具前景的敷料。
要点一:
实验室通过利用多重动态氢键相互作用,将PVA、TA、甘油和释氧CPO NPs整合在一起,制备了一种多功能CPO-PTG水凝胶。CPO-PTG水凝胶具有优异的可注射性和高效的自修复性能,使其适合作为伤口敷料使用。
要点二:
CPO-PTG水凝胶在低温低湿条件下仍表现出有利于伤口敷料开发的粘附特性。这些特性使其能够粘附于不规则或湿润的伤口组织,提示该水凝胶可作为无需绑带或胶带的自给式伤口敷料。
要点三:
CPO-PTG水凝胶凭借其双重功能——同时提供氧气并清除ROS——使细胞存活率显著提升至约87.4%。
要点四:
CPO-PTG水凝胶不仅能清除浮游细菌,还能抑制水凝胶表面生物膜的形成,为冻伤创面提供对抗细菌入侵和生物膜相关感染的潜在保护。
要点五:
通过动物实验证明CPO-PTG水凝胶的多种特性,包括清除活性氧(ROS)、产生活性氧及抗菌活性,表明CPO-PTG水凝胶可作为有效的创面敷料以加速冻伤愈合。
要点六:
CPO-PTG水凝胶敷料在伤口愈合早期阶段调控炎症反应,并在后期阶段显著加速血管生成,从而在14天内促进冻伤伤口的愈合。
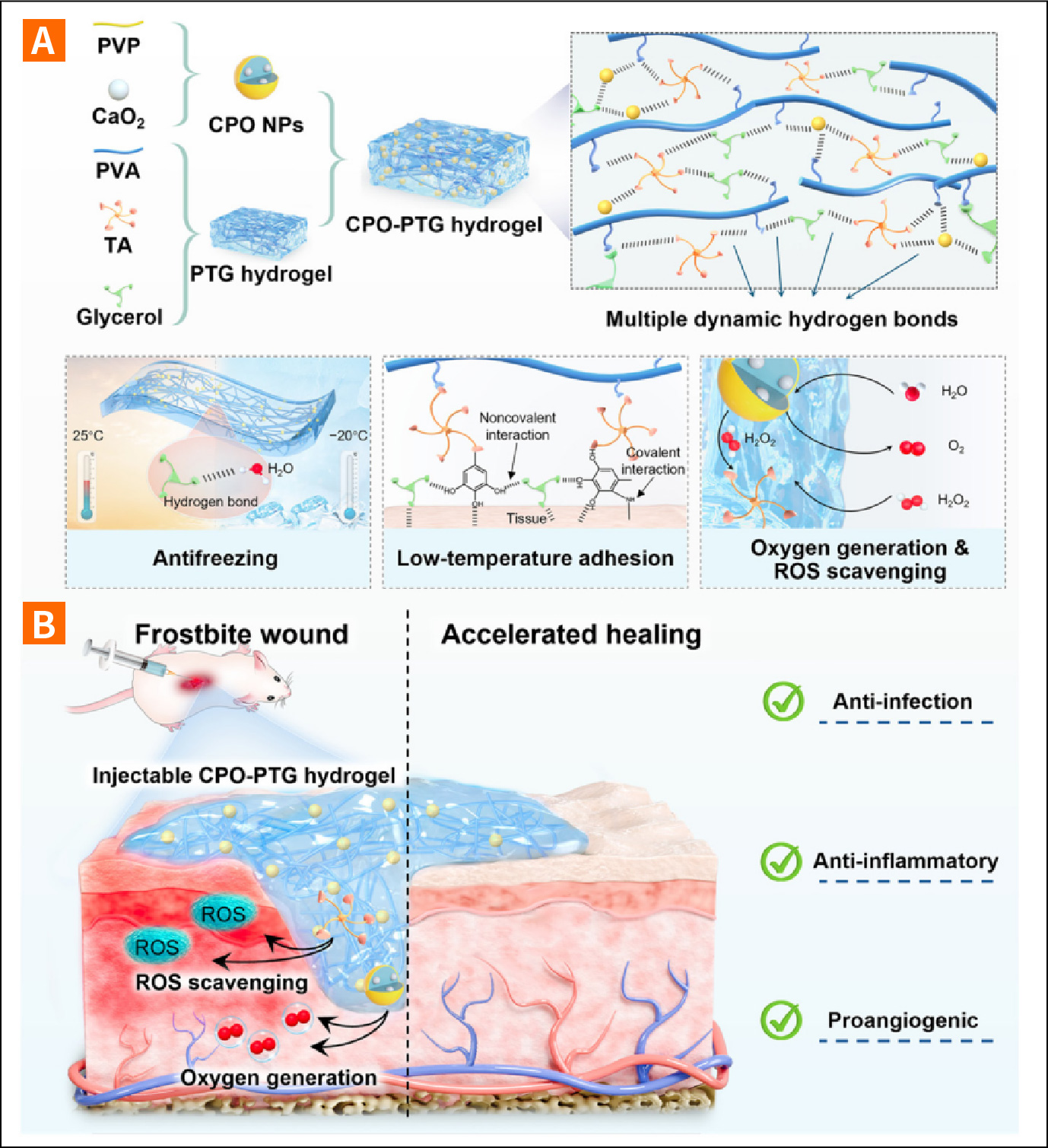
CPO-PTG水凝胶制备及其治疗高海拔冻伤应用的示意图
(A)通过多重氢键相互作用制备CPO-PTG水凝胶,及其抗冻、低温粘附、活性氧清除和产氧特性的示意图。(B)应用可注射CPO-PTG水凝胶敷料通过产氧、活性氧清除、抗菌活性和抗炎作用促进高海拔冻伤创面愈合。
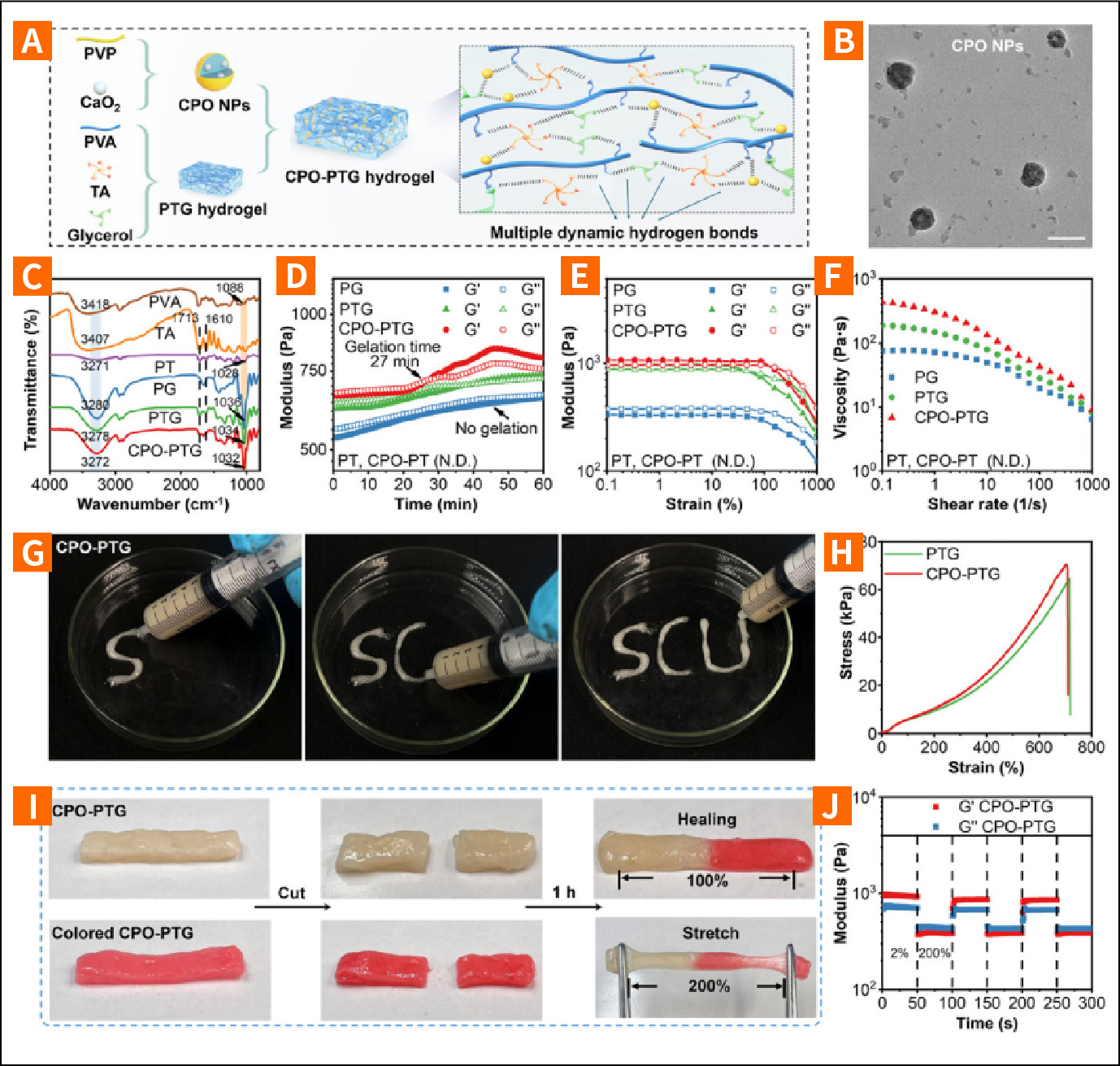
多功能水凝胶的特点
(A) CPO-PTG水凝胶制备过程及水凝胶中多重动态氢键的示意图。(B) CPO NPs的TEM图像。比例尺 = 100nm。(C) PVA、TA、PG、PTG及CPO-PTG水凝胶的FITR光谱。(D)PG、PTG和CPO-PTG水凝胶的频率扫描,(E)应变扫描,以及(F)连续流动测试。由于凝聚层的形成。无法获得PT或CPO-PT的流动曲线。(G) CPO-PTG水凝胶通过注射器注射的数字照片。 (H) PTG和CPO-PTG水凝胶静置27分钟后的拉伸应力-应变曲线。(I) CPO-PTG水凝胶的自修复行为及(J)当交替阶跃应变从2%切换至200%时CPO-PTG水凝胶的流变特性。
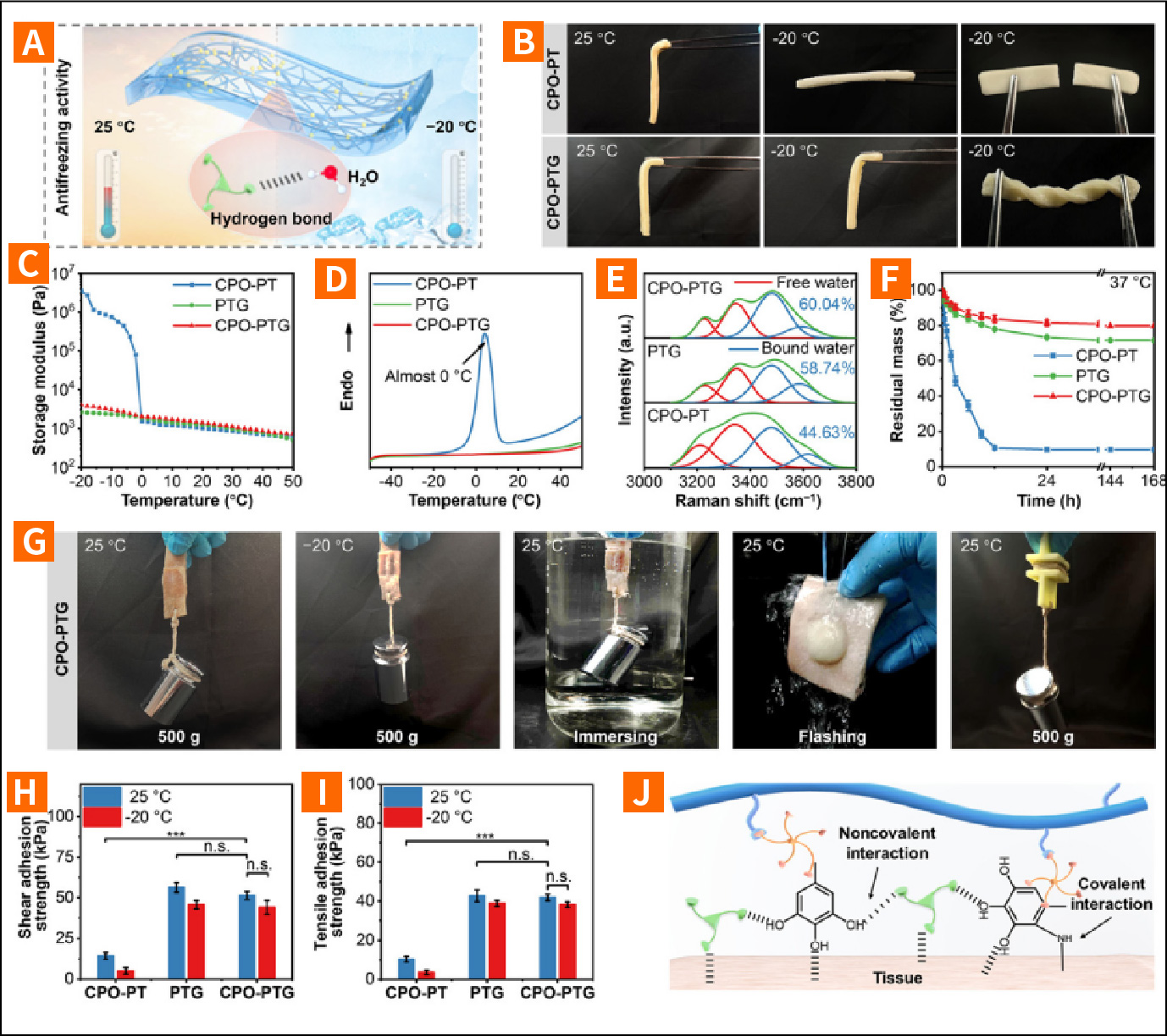
CPO-PTG水凝胶的防冻、保水及粘附性能实验
(A)甘油与水分子间氢键作用的CPO-PTG水凝胶防冻机制示意图。(B) CPO-PT与CPO-PTG水凝胶在25℃(室温)和-20℃(低温)下的数码照片。(C)-20至50℃温度范围内水凝胶的储能模量。(D)-50至50℃温度范围内CPO-PT、PTG及CPO-PTG水凝胶的DSC曲线。(E) CPO-PT、PTG及CPO-PTG水凝胶的罗曼光谱图。(F) 37℃下水凝胶7天后的残留质量。(G) CPO-PTG水凝胶在25℃、-20℃及水下条件下承载500克重物的数码照片。(H)CPO-PT、PTG及CPO-PTG水凝胶的剪切粘附强度与拉伸粘附强度。(J)基于粘性甘油相分离效应及多酚与组织间多重界面相互作用的CPO-PTG水凝胶粘附机制。数据以均值±标准差表示;统计学差异采用单因素方差分析及Tukey事后检验评估;n.s. > 0.05,*p < 0.05,**p < 0.01,***p < 0.001。
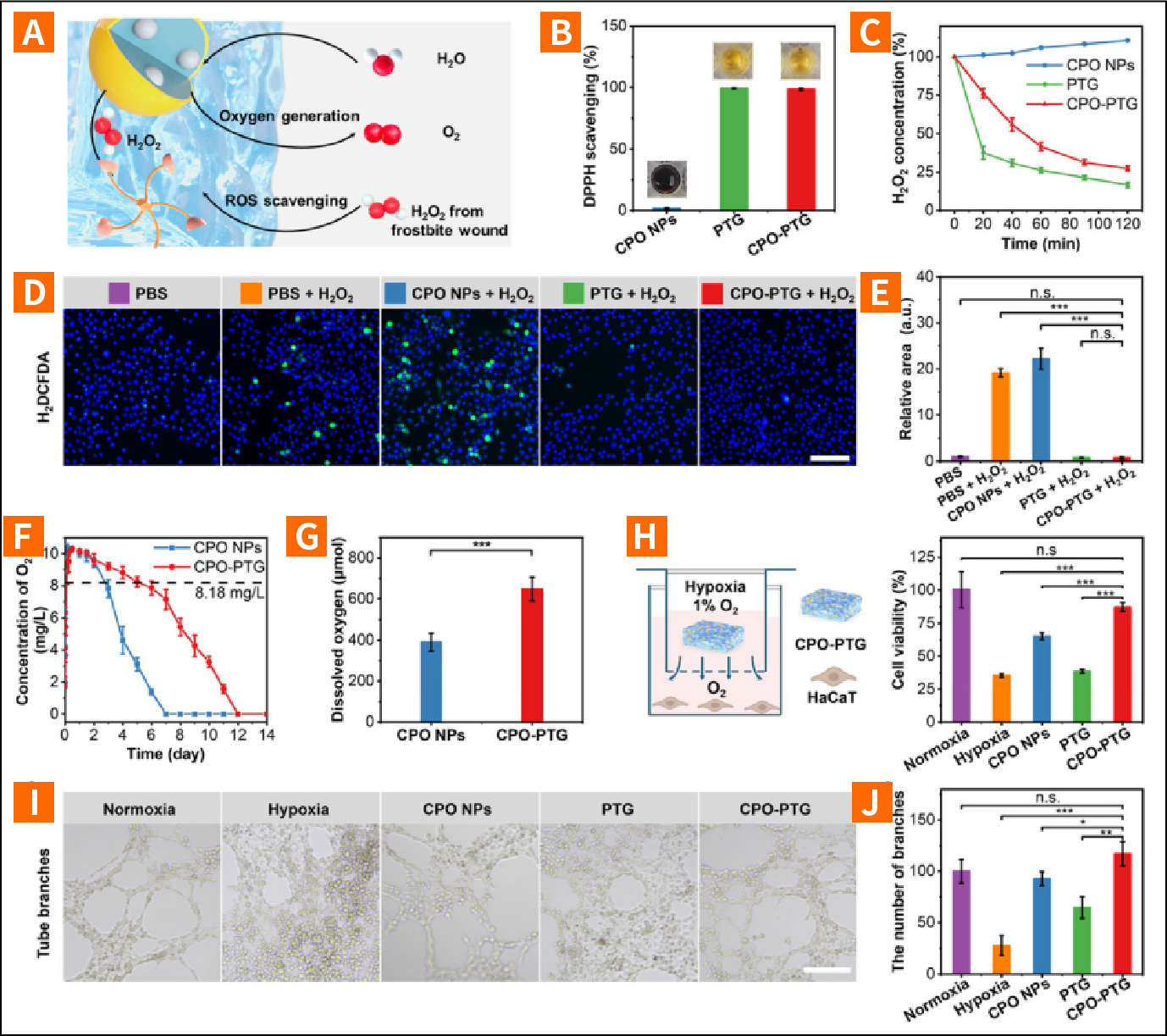
CPO-PTG水凝胶的ROS清除和产氧活性
(A)CPO-PTG水凝胶的ROS清除和产氧机制示意图。(B) DPPH 清除率和(C)残留H2O2浓度。(D) DCFH -DA染色的荧光染色图像及(E)体外含或不含H2O2(100μmol)的HACAT细胞荧光强度分析。比例尺=100μm。(F) CPO NPs和CPO-PTG水凝胶在PBS溶液中12天的氧释放量,以及(G)在PBS溶液中14天的累积O2生成量。(H)体外低氧(1% O2)条件下培养HACAT细胞后,CPONPs、PTG和CPO-PTG水凝胶的细胞活力评估。(I)体外低氧(1%O2)条件下管状结构的代表性图像及(J)分支数量。比例尺=200μm。数据以均值±标准差表示;统计学差异采用单因素方差分析及Tukey事后检验评估;*p<0.05,**p< 0.01,***p < 0.001。
CPO-PTG水凝胶的抗菌性能评估
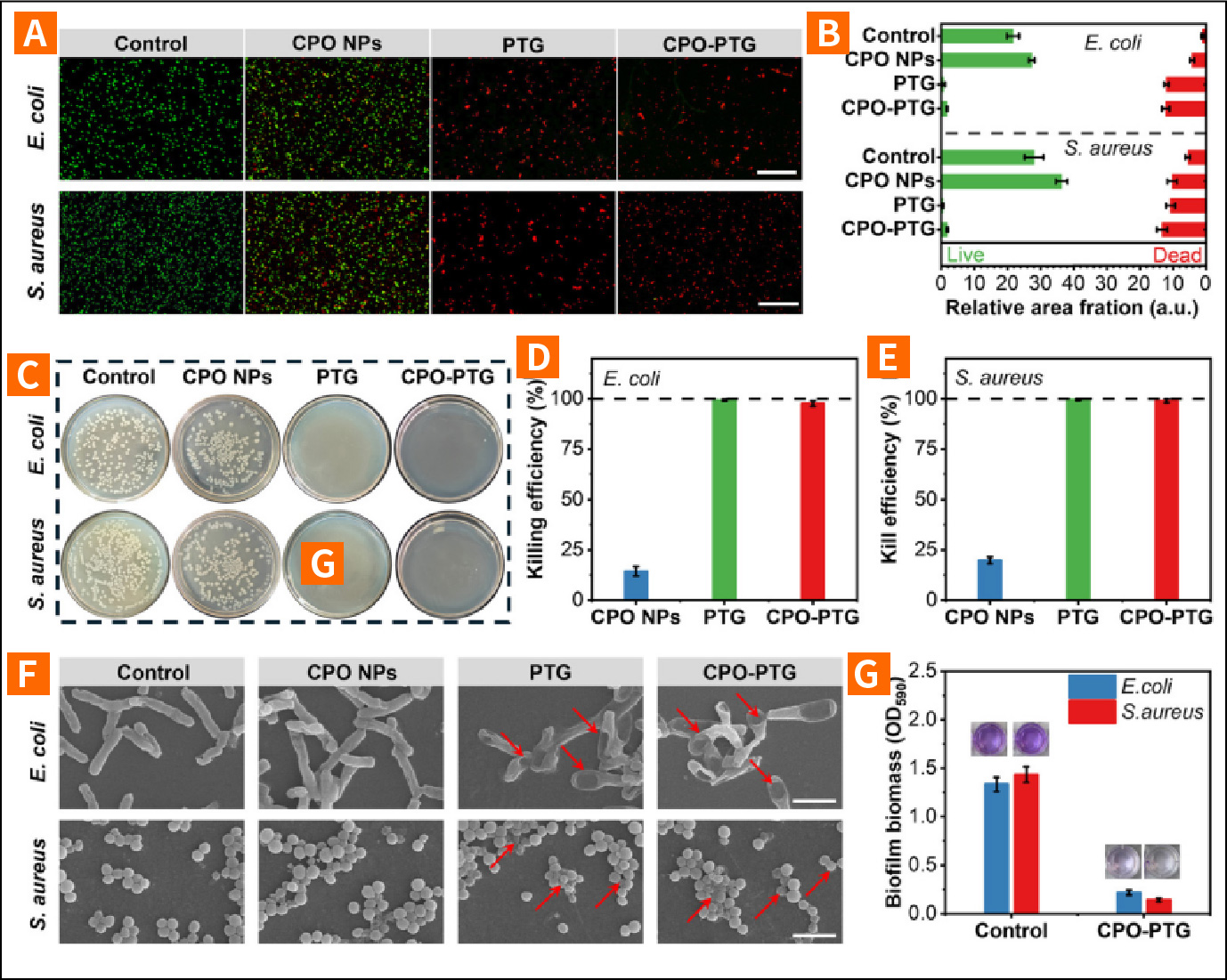
(A)金黄色葡萄球菌和大肠杆菌与PBS溶液、CPO纳米颗粒、PTG及CPO-PTG水凝胶共培养2小时后的代表性活/死细胞荧光图像及(B)红绿荧光相对面积对比。比例尺=100μm。(C)细菌菌落照片及(D)金黄色葡萄球菌、(E)大肠杆菌在琼脂平板接触2小时后的杀菌效率。(F)细菌形态的扫描电镜图像。比例尺=2.5μm。(G)采用结晶紫染色法对细菌孵育14天后的生物膜形成进行定量分析。
SD大鼠体内冻伤创面愈合
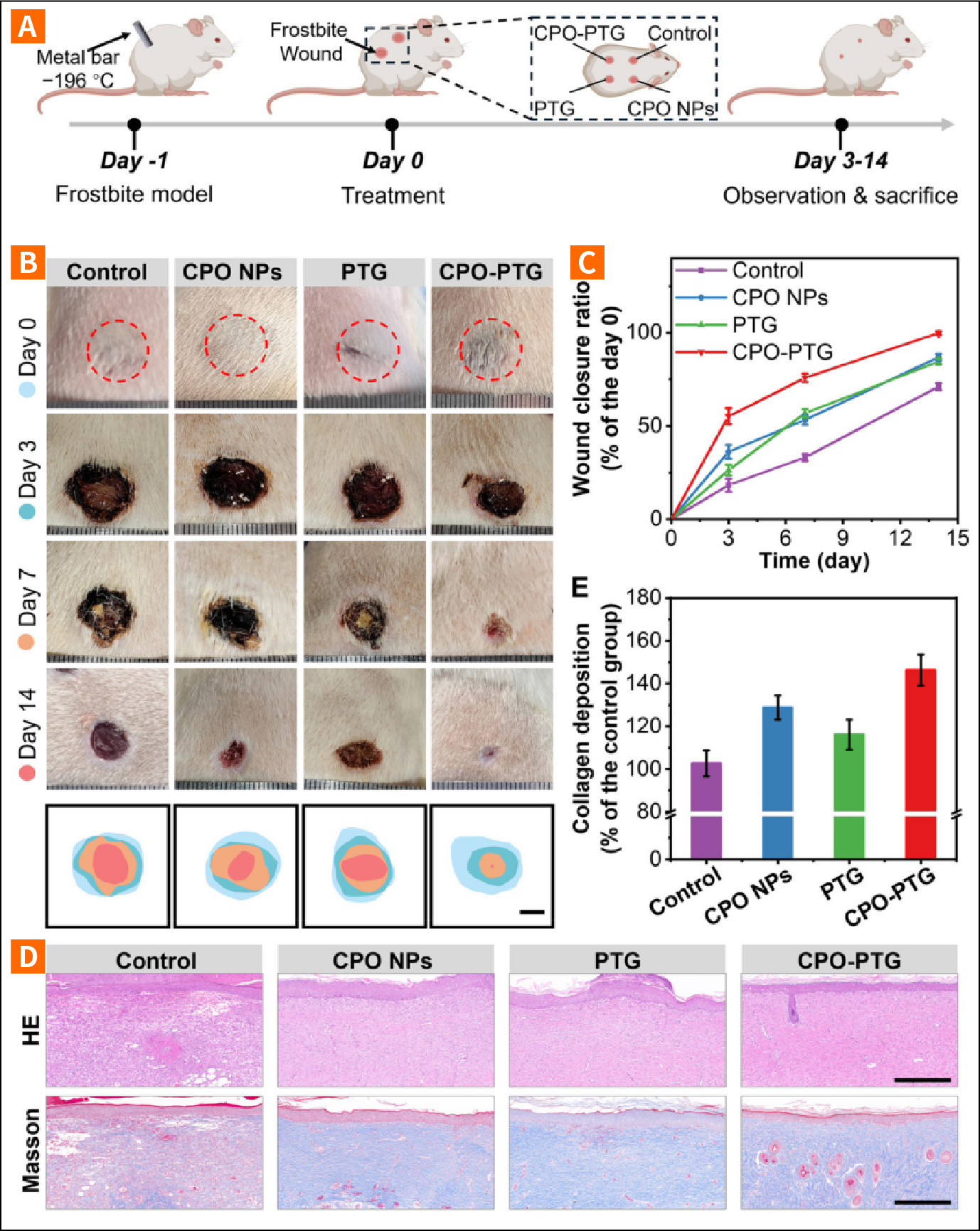
(A) SD大鼠冻伤建立与治疗的示意图。(B)对照组、CPO NPs组、PTG组及CPO-PTG组在第0、3、7和14天的冻伤创面残余区域代表性图像与示意图。比例尺=5mm。(C)与第0天创面面积相比的创面闭合率定量分析。(D)治疗14天后冻伤组织的HE染色与Masson染色图像。比例尺=500μm。(E)与对照组组织相比的组织相对胶原沉积量。
CPO-PTG水凝胶敷料的体内抗炎及促血管生成作用
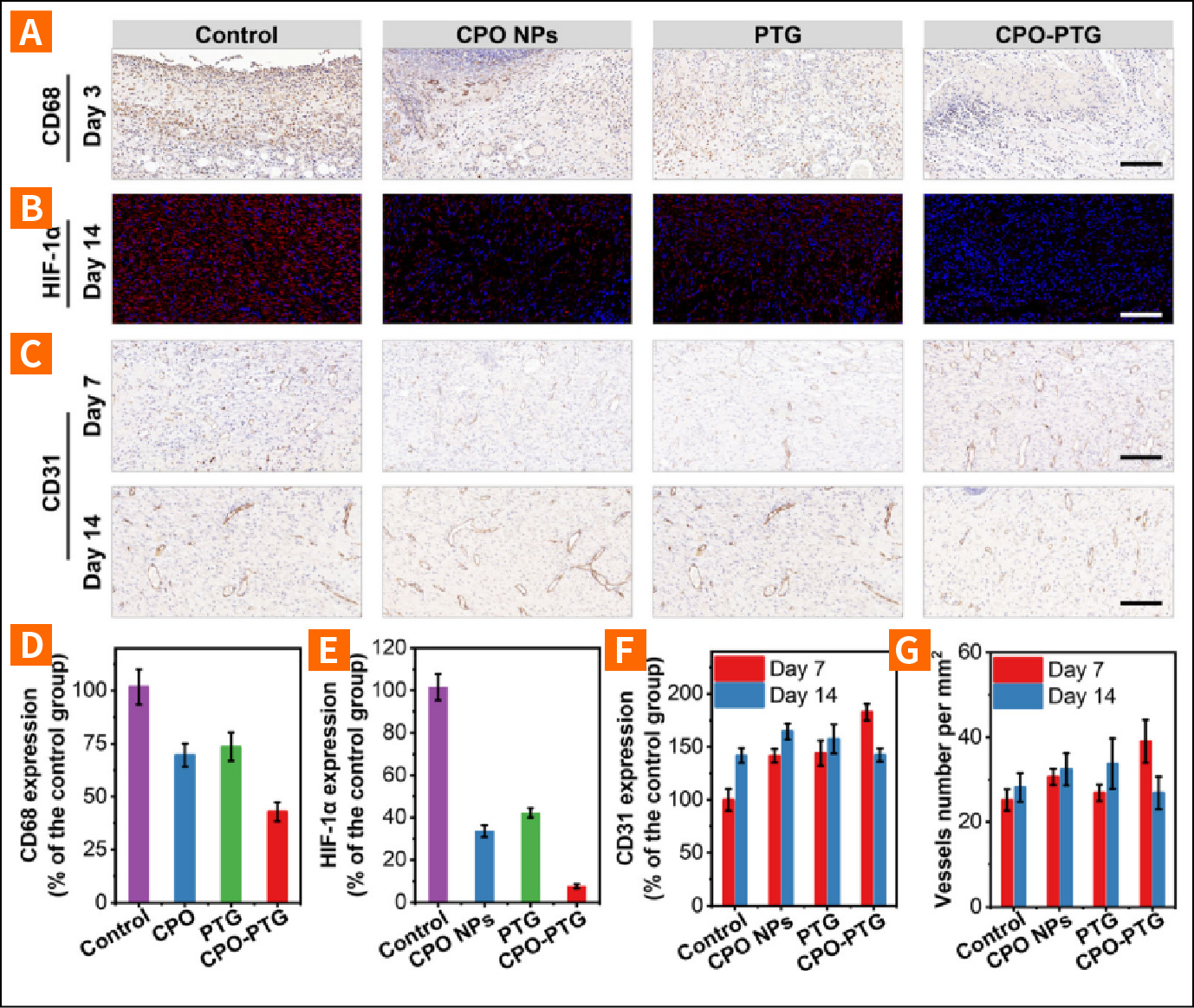
(A)第3天CD68的IHC染色。比例尺=150μm。(B)第7天HIF-1α 的免疫荧光染色。比例尺=150μm。(C)第7天和第14天CD31的IHC染色。比例尺=150μm。(D)对照组、CPO纳米颗粒组、PTG组和CPO-PTG水凝胶组中CD68表达的定量分析。(E)HIF-1α 表达的定量分析。(F)CD31表达与对照组的定量分析。(G)第14天血管数量的定量分析。